
Nous utilisons deux sortes de tensioactifs: les TRITON X 35 et X 100 qui possèdent la même chaîne hydrocarbonée et ne différent que par le nombre de groupes oxyéthylène de leur partie hydrophile: pour le TX 35, on a seulement 3 groupes oxyéthylène alors que pour le TX 100, on trouve 9 groupes -(-CH2-CH2-O-)-. A cause du faible volume de sa tête, le TX 35 ne forme des micelles que s'il est accompagné d'un autre tensioactif à tête plus importante comme le TX 100. C'est pour cela qu'on appelle le TX 35 un cotensioactif.

On verra dans la suite que le choix d'une telle association n'est pas innocent puisqu'on va utiliser les différences entre les paramètres géométriques des deux molécules amphiphiles.
On a vu dans le premier chapitre que dans le cas d'une micelle sphérique, le rayon est voisin de la longueur de chaîne l et on peut calculer le nombre approché de molécules constituantes en divisant le volume de la sphère par v ou sa surface par s, soit N= 4p l^3/3v ou N=4pl^2/s d'où l=3v/s. De sorte que le la condition de formation d'une micelle sphérique s'écrit, en fonction de lc supérieur ou égal à l et du facteur de forme:
Pc = v / (lc s) <1/3
On se sert du facteur de forme pour comprendre le comportement de notre système: l'association des deux TX prend alors tout son sens. En ajustant les concentrations de ces deux composés on peut régler précisément le rayon de la micelle.
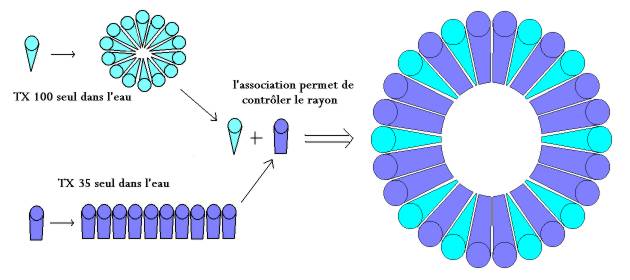
Contrôle du rayon par l'association du TX 35 et du TX 100
Les polymères composants la membrane sont renouvelés avec une fréquence élevée ce qui permet d'assurer que même sur une échelle de temps courte, de 10^-10 secondes, la composition de la membrane reste constante et on obtient une monodispersité des tailles.
Dans nos expériences, nous avons utilisé le polymère formé de groupes polyoxyéthylènes appelé POE ; le nombre de monomères est assez mono disperse et est fixé à 230. On a montré dans le premier chapitre la dépendance du comportement de la chaîne en fonction de la température:
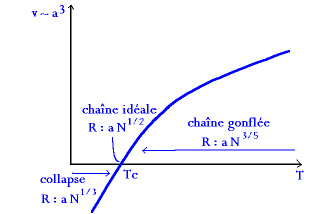
On se place à 20 °C donc d'après les tables la chaîne de POE aura un comportement de chaîne gonflée ; de plus les liaisons hydrogènes entre les molécules d'eau de la solution et les monomères créent une enveloppe autour de la chaîne et justifient le comportement de "bon solvant" et de "chaîne auto-évitante". Nous utilisons un système bien particulier: notre polymère ne se fixe pas de manière covalente et définitive aux vésicules mais les deux chaînes hydrocarbonées de la molécule peuvent pénétrer dans les vésicules et s'en détacher même si la partie attractive tend à lier le polymère à la vésicule. On représente donc notre polymère POE comme deux stickers reliés par une chaîne flexible sans interaction avec la membrane.
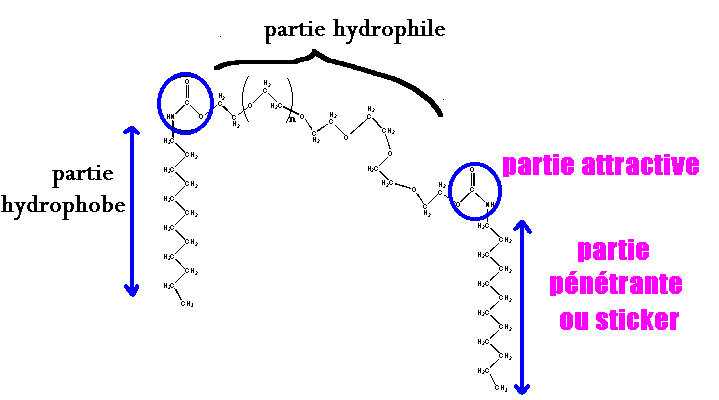
Représentation du polymère POE
Le système change fréquemment de forme, les polymères se connectent et se déconnectent rapidement. On voit ici le rôle très important de la longueur du sticker: plus le sticker est long et plus le temps de résidence dans la micelle est long…Ici on a un sticker en C 12 mais le même système avec un polymère en C 18 est radicalement différent: il est beaucoup plus visqueux.
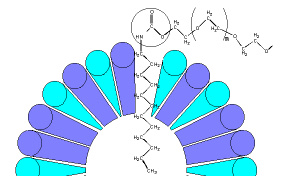
Mode de fixation du sticker dans la micelle
On a donc pour chaque polymère deux solutions: soit le polymère connecte deux micelles différentes, soit les deux stickers se plantent dans la même micelle pour la décorer en "fleur". Le but de l'étude sera donc de déterminer les concentrations limites en micelles et en polymères correspondant aux transitions gel-fleur.
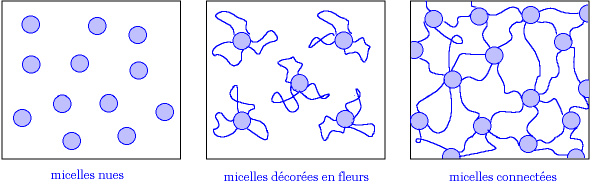
Transition gel-fleurs
Les solutions utilisées dans nos expériences ont été préparées à partir des solutions mères fournies par le Groupe de Dynamique des phases condensées de Montpellier. Toutes ces solutions ont été filtrées à l'aide de filtres millipores de 22 micromètres fixés au bout des seringues dont le bout était dépourvu de joint en caoutchouc (les membres du GDPC ont en effet constaté que le lubrifiant qui permet au piston de coulisser dans le corps de la seringue se retrouvait dans la solution qui devenait trouble au bout de quelques instants). L'étape de filtration est nécessaire pour purger la solution de poussières avant le passage en FRAPP.
On a vu qu'en contrôlant la quantité de TX35 par rapport à celle du TX100, on peut ajuster la courbure du film amphiphile pour donner à la micelle le rayon voulu. Au système TX100+TX35 on ajoute aussi une huile en C10, le décane, qui va prendre place au c¦ur des micelles pour les gonfler permettant ainsi d'obtenir des billes sphériques de rayon identique. Il convient d'ajuster précisément la quantité d'huile par rapport à celle de tensioactif pour que tout le décane ajouté se retrouve bien à l'intérieur des micelles. En effet, une fois que les micelles, gonflées par le décane, auront atteint le rayon maximal autorisé par le rapport cotensioactif/tensioactif choisi, toute quantité d'huile ajoutée en supplément va surnager à la surface de l'échantillon. On distingue donc deux paramètres qui vont permettre de décrire cette microémulsion (on peut parler de microémulsion car le rayon des gouttelettes est voisin de la centaine d'angström). La courbure du film va être fixée, nous l'avons vu, par la quantité de TX35 dans la solution par rapport à celle de TX100. On appellera W le rapport en masse:
W=m(TX35)/m(TX100)
A cette courbure du film amphiphile va correspondre une quantité maximale d'huile qui pourra prendre place au c¦ur de la micelle. Si on appelle $\Gamma$ le rapport en masse huile/tensioactif
G=m(huile)/(m(TX35)+m(TX100))
alors, il va exister un Gmax au delà duquel toute l'huile ajoutée va se retrouver en dehors des micelles. En fait par commodité et par précaution, on se placera toujours légèrement en deçà de ce Gmax. Un tel système a déjà été étudié au GDPC à Montpellier par Mohamed Filali [14]. Sur les bases du travail déjà effectué, les valeurs G=0.7 et W=0.5 ont été adoptées dans toute cette étude. On sait alors d'après des résultats obtenus par diffusion de neutrons, que pour toute concentration en gouttelettes, la décane est bien seulement au c¦ur des micelles et que le rayon des gouttelettes sphériques est de 110Å.
Pour caractériser complètement la micro émulsion, il faut définir d'autre paramètres que G ou W. On va ainsi introduire les paramètres F, HC et r. Il faut d'abord définir un paramètre qui est la concentration en gouttelettes de la micro émulsion. On pourrait utiliser comme paramètre le poids de tous les constituants des gouttelettes par rapport à la masse totale de la solution
F=(m(TX100)+m(TX35)+m(décane))/(m(TX100)+m(TX35)+m(décane)+m(eau))
On utilise une fraction volumique dans la suite. Ceci s'explique par le fait qu'en première approximation, la masse volumique des composants est de l'ordre de 1. Donc, pour préparer les solutions, on peut utiliser une fraction massique.
On préfère caractériser une gouttelette par la masse de son c¦ur aliphatique par rapport à la masse totale de la solution. Dans le c¦ur d'une micelle, on trouve du décane, et les parties hydrophobes des deux tensioactifs, avec, éventuellement l'extrémité fonctionnelle des polymères. Le reste du polymère, et les parties hydrophiles des deux tensioactifs vont se retrouver à l'extérieur du c¦ur hydrophobe (Hydrophobic Core en anglais) des micelles, et vont les décorer. Ainsi, par exemple, le TX100 a une masse molaire de 624g, et sa partie hydrophobe, qui entre dans la composition du noyau dur des micelles a une masse de 189g. Une microémulsion à 10% de HC contiendra 10 grammes de "Hydrophobic Core" pour 100 grammes de solution.
Pour caractériser complètement la microémulsion connectée, les seuls trois paramètres précédents ne suffisent plus. Il faut maintenant introduire une quatrième variable, qui va caractériser le nombre d'extrémités hydrophobes de polymère par gouttelettes de microémulsion. En fait ce paramètre que nous appellerons r, n'est rien d'autre que le double du nombre total de polymères présents dans la solution divisé par le nombre de gouttelettes de microémulsion de cette même solution (le facteur deux vient du fait que les polymères ont deux extrémités hydrophobes).
r=double du nombre de polymères / nombre de gouttelettes de microémulsion
-Le nombre de polymères est le nombre de moles de polymère multiplié par le nombre d'Avogadro.
-On sait calculer à partir des masses volumiques des composants du c¦ur hydrophobes (décane,parties hydrophobes des tensioactifs et des polymères), le nombre de gouttelettes de 110Å de rayon contenues dans la microémulsion.
On peut alors calculer r simplement à partir de la composition du mélange.
Dans un premier temps, une solution mère de micro émulsion sans polymère HC =10% (F=15.6%) a été préparée. (Nous l'appellerons par la suite microémulsion 1). Ensuite, une micro émulsion contenant des polymères a été préparée. La nécessité de devoir filtrer ces solutions avant de les utiliser en diffusion de lumière, et la viscosité élevée de la micro émulsion contenant le polymère obligent à préparer cette solution en deux temps: Tout d'abord une micro émulsion seule identique à la précédente mais beaucoup plus concentrée (HC=20% environ) a été préparée et filtrée. D'un autre côté, le polymère a été mis en solution dans la quantité d'eau nécessaire pour qu'une fois la solution le contenant et la micro émulsion à 20% mélangés, on ait une concentration en billes HC=10%. Ainsi, la micro émulsion et la solution de polymère ont été filtrées chacune de leur côté puis mélangées pour donner une solution mère contenant le polymère ayant les caractéristiques suivantes:
r=30
F=15.6% ou HC=10
G=0.7
W=0.5
En mélangeant une fraction de la solution mère contenant le polymère avec une certaine quantité de la microémulsion 1, on pourra, à quantité de gouttelettes constante, varier la concentration en polymère et donc contrôler la valeur du paramètre r, le nombre d'extrémités hydrophobes de polymères par gouttelette. On peut aussi diluer la microémulsion 1 avec de l'eau pure contenant de la fluorescéine modifiée pour étudier des solutions ayant un HC allant de 0 à 10%.